
Sciences & Société
Soutenance de thèse : Daria ZOTOVA
Deep brain unsupervised anomaly detection model based on multimodality imaging
Doctorante : Daria ZOTOVA
Laboratoire INSA : CREATIS
Ecole doctorale : ED160 EEA
L'épilepsie touche environ 65 millions de personnes dans le monde, nécessitant pour certains une intervention chirurgicale dépendante de la localisation précise de la zone épileptogène. Cette thèse vise à améliorer la détection des lésions épileptogènes via un système de diagnostic assisté par ordinateur (CAD), en utilisant des données neuroimagerie multimodales. Elle propose l'utilisation de réseaux siamois non supervisés avec des modèles SVM à classe unique pour identifier les anomalies dans les scans cérébraux, initialement testés sur des IRM T1 et FLAIR.
Une contribution majeure est le développement de méthodes pour générer des images PET synthétiques à partir de scans IRM T1, améliorant les capacités de détection du système CAD et abordant le défi des modalités manquantes en utilisant ces images synthétiques comme remplacement des données PET réelles. Cette approche permet une intégration multimodale efficace pour la détection de zones épileptogènes.
La première partie de la thèse examine les avancées dans l'apprentissage profond pour l'imagerie médicale et les stratégies d'intégration des données. La seconde partie détaille les expériences sur la synthèse PET et l'amélioration de la performance du modèle CAD avec l'intégration des données PET synthétiques. Ce travail avance le domaine de l'imagerie médicale dans la recherche sur l'épilepsie et propose des pistes pour améliorer la détection des lésions et les résultats chirurgicaux.
Additional informations
-
Amphithéâtre Emilie du Châtelet (Bibliothèque Marie Curie) - Villeurbanne
Recherche
Valvuloplastie mitrale : la chirurgie qui passe la bague au coeur
Le cœur a ses raideurs … Que les chercheurs n’ignorent pas. Avec ses fluides, ses tensions, ses pressions, l’organe de la vie est un système mécanique dont il faut étudier l’intégrité, surtout lorsque l’on y place un corps étranger. Située dans la partie gauche du cœur, la valve mitrale participe au bon fonctionnement de celui-ci, se contractant pour faire passer le sang du ventricule gauche à l’oreillette gauche. Mais parfois, le mouvement s’affaiblit. Pour soulager une valve fatiguée, déficiente dans son rôle mécanique, les chirurgiens peuvent opter pour l’annuloplastie, une intervention consistant à fixer un anneau en polymère sur l’anneau biologique.
Benyebka Bou-Said, enseignant-chercheur au LaMCoS1, se consacre à un projet de réparation de cette pièce du cœur qui fait souvent défaut à travers le projet « RHU Iceland ». Autour d’un consortium d’envergure nationale, ce projet s’apprête à réunir des chercheurs d’entités universitaires, des équipes hospitalières et des experts industriels pour développer une nouvelle solution d’annuloplastie de la valve mitrale. La solution se veut ambitieuse car elle proposera un implant personnalisé et tout-en-un inséré par la veine fémorale, c’est-à-dire depuis la cuisse du patient. Explications avec l’enseignant-chercheur du LaMCoS.
C’est un petit entonnoir d’à peine plus de trois centimètres qui impose un sens unique à la circulation sanguine. La valve mitrale peut régulièrement se trouver endommagée avec le temps et conduire à une dégradation progressive de la fonction cardiaque. Comme un clapet anti-retour, ses mouvements sont soumis au rythme du cœur. Ainsi, ses feuillets s’ouvrent lorsque celui-ci se relâche et se rejoignent quand il se contracte. Cependant, certaines pathologies ou des prédispositions génétiques peuvent affecter son bon fonctionnement. On parle alors « d’insuffisance mitrale » ou de « régurgitation ». Depuis plusieurs années, des formes de chirurgies reconstructrices permettent de réparer l’élément défaillant. Parmi elles, la « valvuloplastie mitrale » qui consiste à fixer un anneau sur la tête de la valve pour assurer son intégrité.
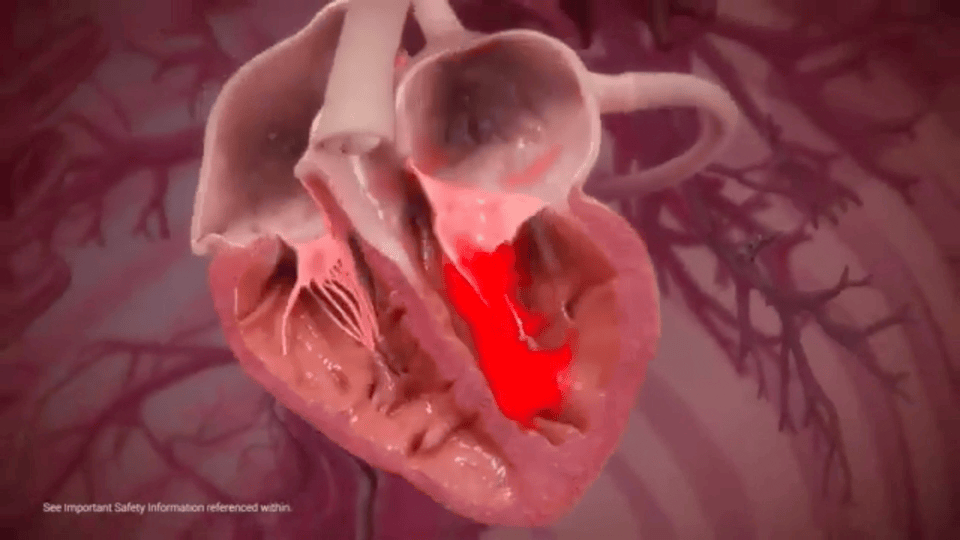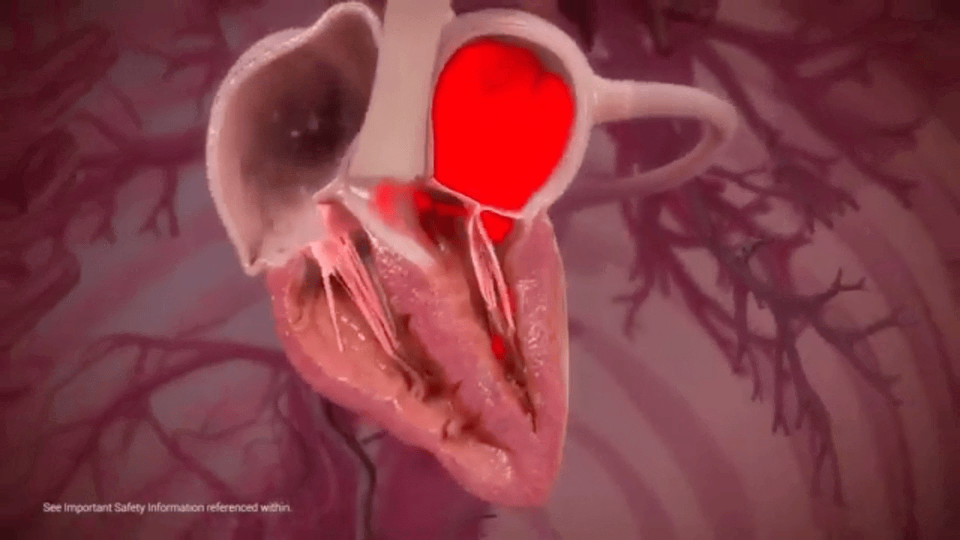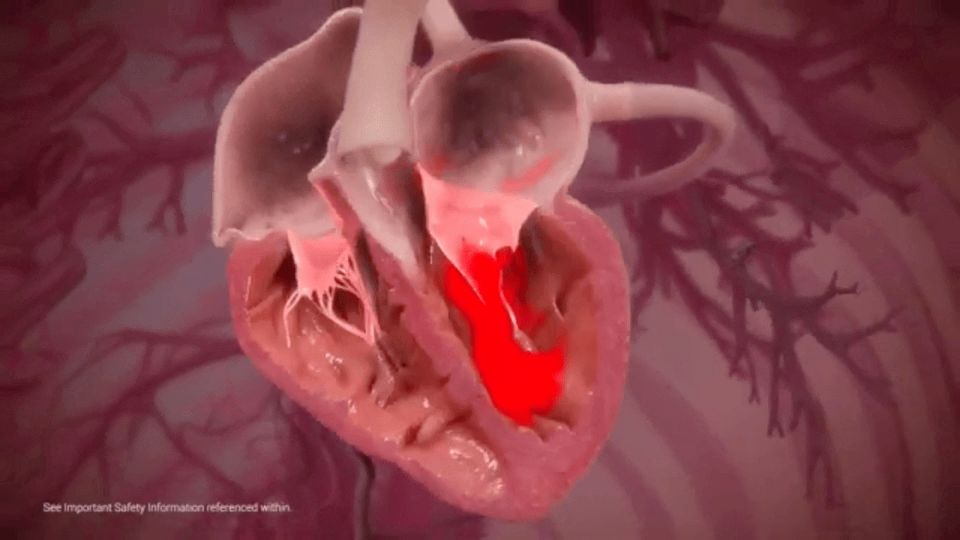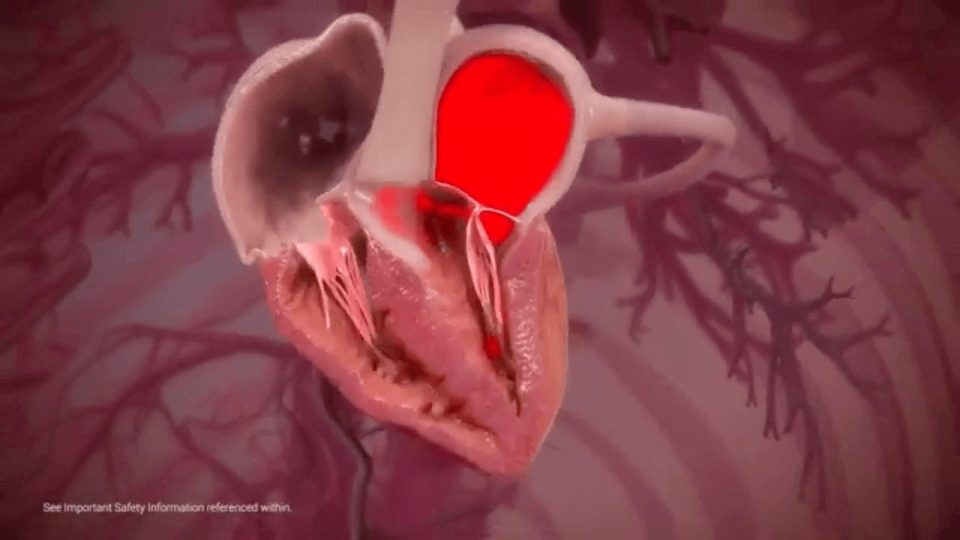
La valve mitrale vit au rythme des mouvements diastoliques (relâchement) et systoliques (contractions) alternatifs de l’organe.
Toucher en plein cœur, depuis la cuisse
 « Aujourd’hui, l’annuloplastie constitue une réfection chirurgicale dont le taux de succès n’est pas optimum et la formation des chirurgiens sur ce type d’intervention est très fastidieuse. Le projet RHU Iceland réunit des universitaires, des équipes hospitalières et un partenaire industriel pour proposer des avancées conséquentes sur la valvuloplastie mitrale », explique Benyebka Bou-Said, enseignant-chercheur à l’INSA Lyon. Et pour proposer des avancées conséquentes, il faut être ambitieux. « Iceland a la prétention de permettre de délivrer l’anneau prothétique à la valve mitrale depuis la cuisse du patient. Dans un même cathéter, l’anneau, les outils de fixations et la sonde d’observation devront monter par la veine fémorale, qui rejoint le côté droit du cœur. Une fois arrivé dans la zone d’intérêt, le tube traversera la paroi de l’atrium droit à l’atrium gauche pour entamer la réparation de la valve », ajoute le chercheur du LAMCoS.
« Aujourd’hui, l’annuloplastie constitue une réfection chirurgicale dont le taux de succès n’est pas optimum et la formation des chirurgiens sur ce type d’intervention est très fastidieuse. Le projet RHU Iceland réunit des universitaires, des équipes hospitalières et un partenaire industriel pour proposer des avancées conséquentes sur la valvuloplastie mitrale », explique Benyebka Bou-Said, enseignant-chercheur à l’INSA Lyon. Et pour proposer des avancées conséquentes, il faut être ambitieux. « Iceland a la prétention de permettre de délivrer l’anneau prothétique à la valve mitrale depuis la cuisse du patient. Dans un même cathéter, l’anneau, les outils de fixations et la sonde d’observation devront monter par la veine fémorale, qui rejoint le côté droit du cœur. Une fois arrivé dans la zone d’intérêt, le tube traversera la paroi de l’atrium droit à l’atrium gauche pour entamer la réparation de la valve », ajoute le chercheur du LAMCoS.
Passer l’anneau à la valve mitrale
Avant que les ancres guidées par le chirurgien ne fixent l’anneau mitral de substitution, il faudra à l’équipe du projet RHU Iceland, développer un implant sûr et robuste. C’est une des missions des chercheurs et doctorantes du LaMCoS impliqués dans le projet. « Pour développer un anneau adaptable à la morphologie de chaque patient, il faudra étudier la rhéologie des matériaux et des tissus biologiques, la durée de vie de la sangle et des agrafes, envisager peut-être une nouvelle forme de l’anneau… Les enjeux scientifiques et techniques pour traiter efficacement l’insuffisance mitrale sur le long terme sont nombreux. C’est un projet transdisciplinaire ambitieux qui occupera dans un second temps, au sein de l’INSA, des collègues du laboratoire MatéIS2 »
Un projet de la médecine 4P : un anneau personnalisé
Puisque chaque cas de chirurgie est différent, l’anneau du projet RHU Iceland se veut être une prothèse personnalisée et adaptable à chaque problématique mitrale. Pour proposer une solution de précision, le projet de recherche hospitalo-universitaire s’appuiera sur l’imagerie médicale pour caractériser les propriétés mécaniques des tissus de chacun des patients. « Avant l’intervention, les équipes médicales étudieront la rigidité, la souplesse et les potentielles réponses des tissus biologiques du patient à partir d’IRM de flux. Cela permettra de pronostiquer les réponses du corps face à une annuloplastie et améliorer ainsi le diagnostic sur la nécessité d’une telle opération », ajoute Benyebka.
Un joystick pour faciliter l’apprentissage chirurgical
Au-delà des difficultés proprement techniques et chirurgicales qu’impose une intervention de cet ordre, l’annuloplastie mitrale soulève un enjeu de formation au geste endovasculaire. Pour faciliter l’apprentissage des chirurgiens novices et résoudre les problèmes éthiques que suscitent les méthodologies actuelles, les chercheurs du LaMCoS et du laboratoire AMPERE se pencheront également sur un simulateur numérique de précision. « L’apprentissage sur joystick existe déjà pour plusieurs types d’opération, mais n’est pas encore appliqué à celle de la valve mitrale. Le simulateur haptique permet de préparer les gestes chirurgicaux de manière précise, grâce à des images statiques et dynamiques. Grâce à la mécanique-robotique, chaque mouvement du joystick devra faire ressentir la réalité biologique au chirurgien apprenant. La manette sera une sorte de traducteur haptique. »
Le programme du projet RHU Iceland s’annonce donc vaste et ambitieux. Les nombreuses équipes impliquées sur le projet espèrent que les premiers résultats, attendus à l’horizon 2027, permettront d’améliorer la prise en charge des patients présentant une valve mitrale défaillante. Affaire à suivre.
Financement ANR : projet sur 5 ans, dotation ANR 5 529 116 Euros
Partenaires : CMINOV – UCBL – INSA Lyon (LAMCOS et MATEIS) – CNRS – Centrale Lyon (LTDS) – Sorbonne Université – CHU St-Étienne
----------
[1] Laboratoire de Mécanique des Contacts et des Structures (INSA Lyon/CNRS/UdL)
[2] MATÉriaux : Ingénierie et Sciences (INSA Lyon/CNRS/Université Lyon 1)
Recherche
La mécanique du cœur : quand la valve mitrale déraille
« Boum-boum. Boum-boum ». Il est certainement l’organe le plus symbolique du corps humain : imprimé sur les cartes de Saint-Valentin, dessiné avec les doigts pour dire son amour à sa moitié derrière une vitre ou même, gravé au compas sur une table de classe, la réalité biologique du cœur est pourtant un peu moins tendre. À peine plus grand que la taille d’un poing fermé, il structure une anatomie extrêmement complexe. Parmi les nombreux éléments qui le compose : la valve mitrale qui impose un sens unique à la circulation sanguine et peut se trouver endommagée avec le temps et conduire à une dégradation progressive de la fonction cardiaque.
Daniel Grinberg est chirurgien cardiaque à l’hôpital Louis Pradel de Bron (HCL), et a récemment soutenu une thèse à l’INSA Lyon. En collaboration avec le laboratoires LGEF1, l’hôpital Mount Sinaï à New York, et son équipe hospitalière au CHU de Lyon, il travaille à l’élaboration d’un outil d’aide au chirurgien pour faciliter les chirurgies valvulaires mitrales et les rendre plus efficaces. Immersion au cœur de la machine.
La valve en bandoulière
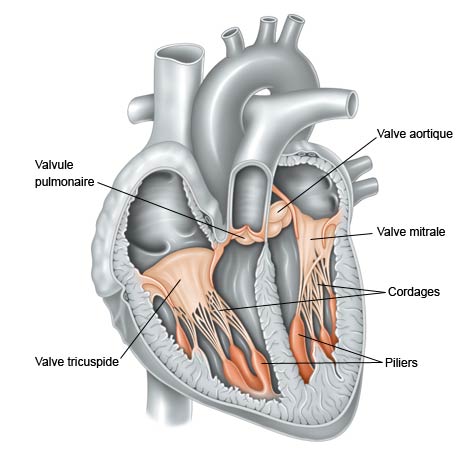
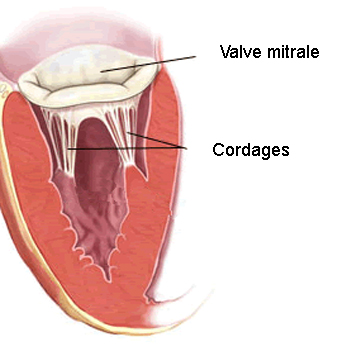
La valve mitrale est l’une des quatre valves séparant les cavités cardiaques qui composent le cœur. Comme un clapet, elle guide le sang, l’empêchant de revenir en arrière. « La valve mitrale se situe entre l’oreillette gauche et le ventricule gauche. Elle ressemble et fonctionne comme un double parachute : quand le cœur se contracte, le sang s’engouffre dans la voilure et les parachutes se gonflent jusqu’à se toucher. C’est ce contact qui forme le clapet antiretour et assure la circulation sanguine et ce, 2 milliards de fois au cours d’une vie humaine ! Dès lors qu’un élément des parachutes est abimé (la voilure, appelée ici « valvule » ou les fils tracteurs, appelés ici « cordages »), la valve mitrale n’assure plus son rôle et le cœur fatigue. Quand la mécanique ne fonctionne plus, il faut opérer, pour au mieux réparer la valve ou bien la remplacer par une prothèse », explique le docteur Grinberg, du service de chirurgie cardiaque adulte à l’hôpital Louis Pradel.
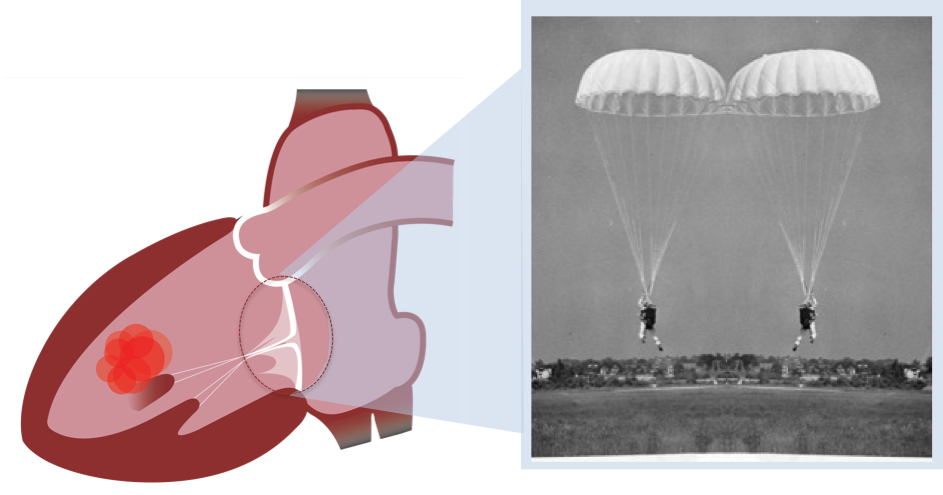
En France, près de 7000 chirurgies valvulaires mitrales sont réalisées chaque année. En cause de la dégénérescence de cet élément : le temps et l’âge. Plusieurs symptômes peuvent être associés à une mauvaise étanchéité de l’orifice mitral. « En matière d’insuffisance mitrale, il existe des traitements pour diminuer les symptômes, mais seule la chirurgie peut résoudre le fond du problème. Cette chirurgie est difficile car nous ne sommes pas en mesure d’évaluer en direct ce qu’il se passe physiquement dans le coeur pendant une opération. Par exemple, lorsque l’on effectue une réparation, on arrête le cœur : il est mou et vide de sang, alors lorsqu’il est remis en route, il se peut que cette réparation ne fonctionne pas aussi bien qu’elle devrait. Il n’existe pas de système à 100% fiable et certains patients reviennent nous voir des semaines, des mois ou des années après l’intervention pour une récidive de fuite. Nous avons donc cherché à développer des outils permettant d’évaluer les changements physiques survenants pendant la chirurgie, qui pourraient nous aider à éviter les récidives », ajoute le docteur.
La rencontre avec le laboratoire LGEF : « It’s a crush ! »
En 2015, lorsque le Dr. Daniel Grinberg et le Pf. Jean-François Obadia viennent frapper à la porte des laboratoires de l’INSA Lyon, ils travaillent déjà à remplacer les cordages rompus par des cordages artificiels en Gore Tex, sans même arrêter le cœur grâce au dispositif NeoChord DS1000®️. « C’est entre deux chirurgies et autour de quelques sandwichs que nous avons fait connaissance avec Pierre-Jean Cottinet, enseignant-chercheur à l’INSA Lyon et au LGEF, qui est par la suite devenu mon ami et mon directeur de thèse. Nous avons amené la première problématique : comment mesurer la tension qui s’exerce sur ces cordages artificiels pendant l’opération ? Cette question n’a été que la première d’une longue série », poursuit Daniel.
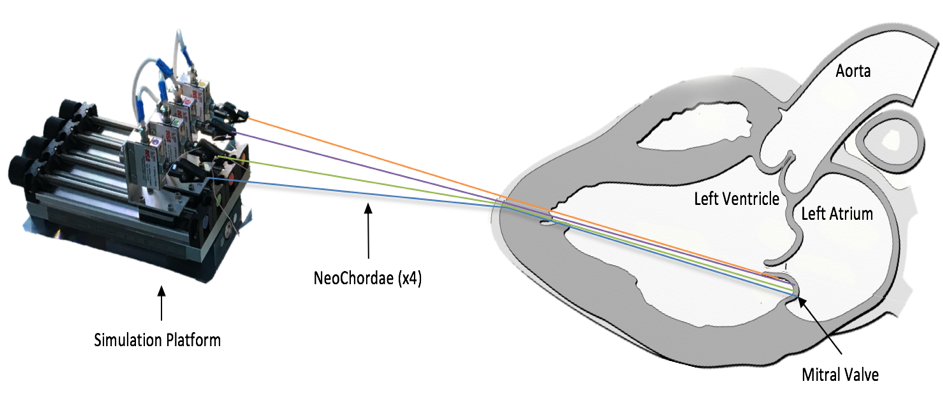
De fil en aiguille, les médecins et les chercheurs de l’INSA Lyon parviennent à développer un banc d’essai : c’est la première fois qu’il est possible de mesurer chez l’homme, à cœur battant et pendant une opération chirurgicale, la tension exercée sur les cordages mitraux. Le banc d’essai développé, désormais breveté2, a fait l’objet de différentes publications scientifiques et salué par les experts du domaine. Mais les chercheurs et médecins ne s’arrêtent pas là. « Les données récoltées par notre banc d’essai étaient totalement inédites et nous ont permis de mieux comprendre les maladies mitrales et les conséquences de la chirurgie. Mais après ces observations faites, il s’agissait de les comprendre. Nous avons débuté une collaboration avec des laboratoires spécialisés en imagerie médicale et en simulation numérique dont le laboratoire CREATIS3, pour créer et optimiser des modèles de « cœur numérique » et ainsi, essayer de comprendre les facteurs influençant la tension des cordages. Nous sommes encore en train de travailler sur le phénomène à travers un projet ANR intitulé ‘SIMR’. »
Le cœur à l’ouvrage
Parmi les autres paramètres capables d’influencer la qualité de l’étanchéité de la valve mitrale, il y a la coaptation, qui correspond à la force de contact entre les deux parachutes composant la valve. « La coaptation est la force que ces deux valvules ont à se fermer l’une contre l’autre et cette force conditionne l’étanchéité de la valve. C’est le sujet du second outil que nous avons développé et breveté pendant mon travail de thèse au LGEF. Nous voulons que cet outil puisse d’une part nous aider à comprendre les maladies et les conséquences de la chirurgie mitrale, et d’autre part, en faire un appareil qui permette d’assister le chirurgien pendant son intervention », poursuit-il.

Dans le cadre de sa thèse, Daniel Grinberg s’est envolé pour New York, à l’hôpital du Mont Sinaï. « Au sein de cet hôpital, que l’on peut considérer comme le ‘temple’ de la valve mitrale, nous avons réussi à jeter les bases d’une première version de l’outil, avec des tests in-vivo et ex-vivo sur des cœurs de porcs. Depuis mon retour en France, nous avons avancé sur l’amélioration de l’outil qui permet désormais de mesurer les forces de coaptation directement sur un cathéter, pendant des interventions à cœur battant. C’est une vraie avancée pour la chirurgie mini-invasive », se réjouit le médecin.
Aujourd’hui, les nombreux scientifiques engagés dans ces deux projets poursuivent leurs recherches. Grâce à des liens renforcés entre les laboratoires de l’INSA Lyon, les Hospices Civils de Lyon et l’hôpital new yorkais, Daniel Grinberg a bon espoir de voir un appareil apparaître dans les prochaines années. « En tant que médecin, je me dois de garder les pieds sur terre et ne pas vendre de la poudre de perlimpinpin. Il reste encore beaucoup de travail avant de pouvoir fournir aux chirurgiens cardiaques et aux cardiologues, un outil utile, efficace et règlementaire pour rendre les interventions sur les valves mitrales plus sûres. Mais il est certain que les résultats de ces travaux sont déjà prometteurs et inédits dans le domaine de la médecine valvulaire mitrale », conclut-il.
 Le développement du banc d’essai de mesure de la tension exercée sur les cordages artificiels au cours des procédures NeoChord®️ avait bénéficié en 2019 du soutien d'INSAVALOR, via un BQI (bonus qualité innovation). Ce dispositif a été un appui à ce projet innovant en permettant de faire la « preuve du concept » pendant un an.
Le développement du banc d’essai de mesure de la tension exercée sur les cordages artificiels au cours des procédures NeoChord®️ avait bénéficié en 2019 du soutien d'INSAVALOR, via un BQI (bonus qualité innovation). Ce dispositif a été un appui à ce projet innovant en permettant de faire la « preuve du concept » pendant un an.
1 LGEF : Laboratoire de Génie Électrique et Ferroélectricité (INSA Lyon)
2 EP18157633 – INSA Lyon/Université Lyon1/Hospices Civils de Lyon – dépôt via la SATT Pulsalys
3 Centre de recherche en Acquisition et Traitement d’Images pour la Santé (INSA Lyon/Lyon1/UJM)
4 L’Agence Nationale de la Recherche finance la recherche publique et la recherche partenariale en France

Recherche
Robotique chirurgicale : Bertin Nahum œuvre pour sauver des vies
Bertin Nahum aura une révélation au cours de sa formation à l’INSA Lyon : il sauvera des vies. Depuis, il transforme ses rêves en objectifs et s’apprête à lancer sur le marché Epione®, un robot capable d’assister les chirurgiens dans le traitement du cancer du foie. Parcours d’un homme qui a révolutionné la chirurgie grâce à la robotique.
Ingénieur diplômé de l’INSA en 1994, vous aviez choisi le département Génie Électrique. Comment en êtes-vous venu à poursuivre la voie de la robotique chirurgicale ?
C’est à la fin de mon cursus à l’INSA Lyon, lors d’un projet de fin d’études en collaboration avec l’hôpital de neuro-cardiologique, que l’immersion dans le milieu médical a été une révélation. Nous devions développer un logiciel d’intelligence artificielle pour faire le diagnostic automatique de lésions crâniennes. Jusque-là, mes choix se faisaient plutôt par défaut. Dès lors, pouvoir contribuer à soigner les gens a donné du sens à mon diplôme d’ingénieur en génie électrique et électronique. Et j’ai voulu consacrer mes compétences et mes connaissances aux technologies dédiées à la santé.
Vous être réputé comme étant l’un des entrepreneurs high-techs les plus innovants au monde. Quel regard portez-vous sur votre parcours ?
J’éprouve à la fois de la satisfaction et une certaine fierté concernant mon parcours professionnel.
Mon leitmotiv depuis des années est la volonté de révolutionner la chirurgie en misant sur la robotique.
Grâce à ma force de conviction, j’ai réussi à créer une première entreprise Medtech S.A en 2002 et développer ainsi Brigit, un robot destiné à la chirurgie orthopédique, puis Rosa, un robot dédié aux opérations du cerveau et de la colonne vertébrale.
En 2013, j’ai fait l’introduction en bourse de cette société puis je l’ai accompagnée dans son rachat en 2016 au prix de 165 millions d’euros par le groupe américain Zimmer Biomet Robotics, leader mondial des implants orthopédiques.
En 2017, je réussis à convaincre certains collaborateurs de co-fonder Quantum Surgical et de se lancer dans une nouvelle aventure à mes côtés.
Je pense que ma détermination est un élément essentiel concernant mon parcours. C’est cette confiance en mes projets et cette détermination qui m’amènent la réussite, et surtout m’aident à surmonter les échecs, inévitables, de la vie d’entrepreneur.
Vous venez de terminer les essais cliniques d’un robot chirurgical dédié au traitement du cancer du foie. Pourquoi cette spécialisation ?
Mon équipe et moi-même nous sommes orientés vers le cancer du foie car c’est le 6e cancer le plus répandu dans le monde, et le 2e en termes de mortalité.
Cette pathologie touche 840 000 nouveaux patients chaque année dans le monde dont 8 000 en France. De plus, les métastases hépatiques concernent trois fois plus de patients (2,4 millions de nouveaux patients chaque année à travers le monde).
Fort de ce constat, nous avons décidé de créer notre robot Epione® permettant ainsi d'assister les praticiens dans leurs gestes, de réduit l'impact des opérations, les risques d'infection et les durées d'hospitalisation.
En ces temps confinés où il est parfois difficile de rester optimiste, quel message pourriez-vous faire passer ?
Je pense que cette crise nous permet de nous réinventer. Il est important de continuer de croire en son projet et ne pas s’arrêter.
Copyright photo : Quantum Surgical
Podcasts « Les cœurs audacieux » - Saison 2 / Épisode 1 - 27 octobre 2021

